- -10%

Indications thérapeutiques:
Le traitement de l'oedème des jambes d'origine veineuse et des symptômes liés à une insuffisance veineuse chronique, tels que jambes lourdes et douloureuses, et gonflements.
Le traitement adjuvant des hémorroïdes internes à court terme.
Composition qualitative et quantitative:
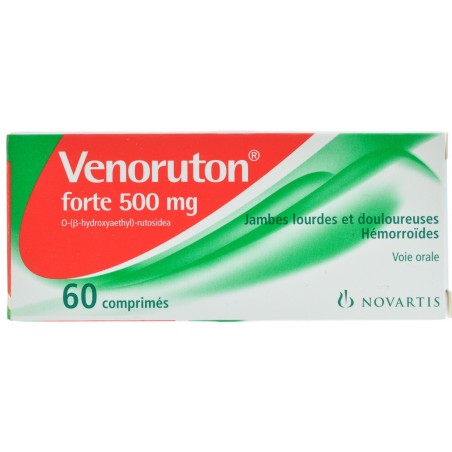
Venoruton forte 500 mg comprimés: un comprimé contient 500 mg d'O-(-hydroxyaethyl)-rutosidea (HR); Venoruton 300 mg gélules: une gélule contient 300 mg d'O-(-hydroxyaethyl)-rutosidea (HR); Venoruton sachets 1.000 mg poudre pour solution buvable: un sachet contient 1.000 mg d'O-(-hydroxyaethyl)-rutosidea (HR).
Pour les excipients, cf. § "Liste des excipients".
Formes pharmaceutiques:
Venoruton forte 500 mg comprimés: comprimé circulaire, biconvexe, marbré, jaune-verdâtre, pour administration orale; Venoruton 300 mg gélules: gélule de gélatine dure, opaque, jaune-beige, pour administration orale; Venoruton sachets 1.000 mg poudre pour solution buvable: poudre granuleuse jaune, pour administration orale après dissolution dans un verre d'eau.
Posologie et mode d'administration:
Il est recommandé de prendre Venoruton au moment des repas.
Venoruton forte 500 mg comprimés, Venoruton sachets 1.000 mg poudre pour solution buvable, Venoruton forte 500 mg, Venoruton sachets 1.000 mg sont surtout destinés au traitement d'attaque des symptômes liés à l'insuffisance veineuse chronique (IVC).
Le traitement est poursuivi jusqu'à disparition des symptômes (habituellement après 6 à 12 semaines, selon la gravité des symptômes).
Une diminution des symptômes devrait normalement s'observer dans les 2 semaines.
Venoruton forte 500 mg: 2 comprimés par jour.
Venoruton sachets 1.000 mg: Dissoudre complètement la poudre contenue dans le sachet dans de l'eau, en remuant bien: 1 sachet par jour, à dissoudre dans un verre d'eau entier.
Il est recommandé de poursuivre le traitement avec Venoruton 300 mg pour consolider les résultats obtenus. La posologie de consolidation utilisée sera, dans la plupart des cas, 2 gélules de Venoruton 300 mg par jour.
Venoruton 300 mg gélules: La posologie est généralement de 3 gélules par jour. Cependant, Venoruton 300 mg est surtout destiné à relayer le traitement d'attaque instauré avec Venoruton forte 500 mg ou Venoruton sachets 1.000 mg. Dans ce cas, la posologie sera généralement de 2 gélules par jour.
Pour certains patients, la posologie de consolidation pourra être fixée de façon individuelle.
?
Contre-indications:
Hypersensibilité à la substance active ou à un des excipients.
Mises en garde spéciales et précautions particulières d'emploi
Le traitement par phlébotrophes ne doit pas être poursuivi pendant plus de 3 mois sans ré-évaluation de la symptomatologie.
Les patients souffrant d'oedème des membres inférieurs suite à des troubles cardiaques, rénaux ou hépatiques ne devraients pas utiliser Venoruton, parce que l'effet de Venoruton n'a pas été démontré dans ces indications.
Grossesse et allaitement:
Un total de 1.431 femmes enceintes ont été traitées avec HR lors de 22 études cliniques différentes. Le dosage journaliers s'échelonnait, dans la plupart de ces études, entre 600 et 1.500 mg (avec des extrêmes de 300 à 3.000 mg). La durée de traitement dans la plupart de ces études était de 2 à 4 semaines, avec un maximum de 5 à 6 mois dans 2 de ces études. Lors de ces études, aucune anomalie fétale n'a été rapportée, qui puisse être attribuée à la prise de Venoruton.
Cependant, comme pour beaucoup de médicaments, l'administration de Venoruton pendant les trois premiers mois de la grossesse est déconseillée.
Lors d'études animales, des traces de HR ont été trouvées dans les foetus et dans le lait maternel. Ces quantités infimes de HR ne sont pas cliniquement significatives.
Effets indésirables:
Occasionellement, de faibles effets indésirables ont été signalés: allergies cutanées, maux de tête, flush et troubles gastro-intestinaux légers.Ils disparaissent rapidement après l'arrêt du traitement.
?
Effets sur l'aptitude à conduire des véhicules et à utiliser des machines:
Il n'y a pas d'indications que le Venoruton pourrait influencer l'aptitude à conduire des véhicules et à utiliser des machines.
Surdosage: Aucun cas de surdosage n'a été signalé à ce jour.
Liste des excipients:
Venoruton forte 500 mg comprimés: Glycol de polyéthylène — Stéarate de magnésium pour un comprimé.
Venoruton 300 mg gélules: Glycol de polyéthylène — Gélatine — Dioxyde de titane — Oxyde de fer jaune pour une gélule.
Venoruton sachets 1.000 mg poudre pour solution buvable: Mannitol — Saccharine sodique — Arôme d'orange pour un sachet.
Interactions avec d'autres médicaments et autres formes d'interactions:
Aucune interaction médicamenteuse n'a été signalée.
Il a été démontré que Venoruton n'a pas d'interactions avec les anticoagulants warfariniques.
Les composants du principe actif sont dérivés de la rutine et de la quercétine. La rutine n'inhibe rien de particulier. La quercétine inhibe le CYP3A hépatique humain et la sulphotransférase in vitro, mais pas in vivo. Pour cette raison, il est admis que l'O-?hydroxyéthyl)-rutosides oral ne produit pas d'effets inhibiteurs ni d'interférence avec le métabolisme d'autres substances pharmacologiquement actives.
Incompatibilités: Pas d'application.
?
Achat médicament en ligne - Le conseil de votre pharmacien:
Le produit Venoruton Forte 500 Comprimés 60 X 500mg est fabriqué (et/ou distribué) avec les plus hauts standard de qualité par la firme NOVARTIS CONSUMER HEALTH. Le site Pharmonet, fort de son expérience dans la vente de produits de qualité, vous propose ici tous les produits disponibles sur le marché de cette marque.
Si néanmoins le produit Venoruton Forte 500 Comprimés 60 X 500mg venait à ne plus vous satisfaire pour quelque raison que ce soit, n'hésitez pas à nous faire part de votre mécontentement et nous nous proposons de reléguer vos remarques directement auprès de la firme NOVARTIS CONSUMER HEALTH.